曾振灵教授课题组在抗生素耐药性方面取得新成果
近日,广东省兽药研制与安全评价重点实验室曾振灵教授课题组在《Environment International》(JCR一区,影响因子7.297)发表了题为“Metagenomic insights into the distribution of antibiotic resistome between the gut-associated environments and the pristine environments”的研究论文(链接 https://www.sciencedirect.com/science/article/pii/S0160412018331660 )。本论文是继该课题组于2018年在《Microbiome》(JCR一区,影响因子9.133)发表的题为“Antibiotic-mediated changes in the faecal microbiome of broiler chickens defines the incidence of antibiotic resistance genes”的研究论文(链接 https://microbiomejournal.biomedcentral.com/articles/10.1186/s40168-018-0419-2) 后的又一重要成果。
农业养殖活动促进了耐药基因的发生和传播。已证实养殖动物肠道、人类肠道、土壤等环境介质是耐药基因的贮存库。这些特定环境中的耐药基因可以被临床病原菌捕获,使重要感染性疾病难以治愈。例如,近年来发现携带有KPC-2、NDM-1 和 MCR-1等耐药机制的超级细菌,严重威胁公共卫生安全。
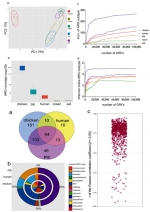
本论文运用宏基因组学技术分析了137个耐药基因组在不同环境介质中的分布特征。发现肠道相关环境中耐药基因的总体丰度显著高于自然环境,耐药基因污染严重程度依次为鸡肠道、猪肠道、人类肠道、海洋和土壤环境。鸡、猪和人类肠道样品中高达64种耐药基因完全一样,且生猪和人肠道耐药基因组结构组成极其相似,表明耐药基因可能具有从养殖动物向人跨界传播的能力。我们通过序列组装,发现在肠道相关环境中Escherichia、Bacteroides、和Clostridium是携带耐药基因最主要的菌属,而在自然环境中Alteromonas、Vibrio和Proteobacteria是携带耐药基因最主要的菌属。在肉鸡肠道,Escherichia主要携带多重耐药、四环素、大环内酯-林酰胺-链阳霉素(MLS)和氨基糖苷类耐药基因;在人和生猪肠道,MLS主要由Bacteroides携带。环境中高达99%的微生物无法在实验室条件下通过传统培养皿进行分离培养。曾振灵教授课题组首次运用宏基因组学技术分析了不同环境介质中耐药基因携带菌的多样性。结果表明,由于微生物在不同环境中所处的生态位不同,导致耐药基因及其携带菌属的分布各异。
我校兽医学院硕士研究生曾佳雄和潘宇为该论文的并列第一作者,曾振灵教授和熊文广副教授为共同通讯作者。本研究得到了国家重点研发计划、国家自然科学基金的资助。(文/图 兽医学院 熊文广)
(责任编辑:蒙丽)