钟南山团队构建全球首个新冠肺炎非转基因小鼠模型
大洋网讯 6月12日,广州市人民政府新闻办公室举办广州市第125场疫情防控复工复产新闻发布会(广州抗疫力量发布专场)。呼吸疾病国家重点实验室副主任赵金存在会上公布,在钟南山院士指导下,其团队成功构建全球首个新冠肺炎非转基因小鼠模型,这一动物模型可应用于新冠治疗药物效果评价、疫苗效果测试及新冠致病机制等多方面研究,有效缓解了我国新冠肺炎动物模型缺乏的难题。该研究成果已于6月10日在线发表于国际顶级期刊《细胞》。
赵金存表示,该项成果也是广东全省大协作的成果,广州医科大学附属第一医院/呼吸疾病国家重点实验室赵金存教授团队外,合作团队还有广州海关技术中心国家生物安全检测重点实验室(P3实验室)、美国爱荷华大学、广州再生医学与健康广东省实验室、中国科学院广州生物医药与健康研究院等。
利用腺病毒载体解决科学难题,小鼠感染后临床表现类似新冠病人
呼吸疾病国家重点实验室副主任赵金存介绍,虽然广州早在疫情早期的2月初已完成毒株分离,但是由于氨基酸关键位点差异,小鼠同源受体mouse ACE2不能介导病毒入侵。而传统受体转基因小鼠模型虽然可作为新冠肺炎研究动物,但由于保有量有限,繁育耗时长,临床症状不典型,造成我国新冠肺炎诊疗方案、药物、疫苗和致病机制体内验证滞后。
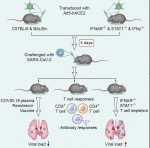
图1. 动物模型模式图
团队采用腺病毒载体来表达新冠肺炎病毒入侵人体的受体,并且通过转导的方式转移到小鼠肺部,让小鼠可以对新冠病毒易感,成功解决了氨基酸关键位点差异的科学难题,建立国际首个非转基因新冠肺炎小鼠动物模型(见图1)。小鼠在新型冠状病毒感染后,肺脏中可检测到高滴度新冠病毒,每克组织中病毒滴度可达107 PFU,并出现体重下降和类似新冠肺炎病人的临床病理表现(见图2)。
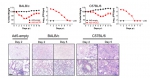
图2. 受体转导小鼠感染SARS-CoV-2后,病毒在小鼠肺脏高滴度复制,小鼠体重下降,肺脏出现出血、炎性细胞浸润等病理改变。
实验显示康复者血浆治疗有效,且病理损伤减轻
团队进一步通过对比野生型小鼠与I型干扰素受体缺陷小鼠和干扰素通路关键基因STAT1敲除小鼠在新型冠状病毒感染后的差异,发现I型干扰素在新冠病毒感染中起到保护作用。
此外,在此模型中,新冠病毒感染可诱导机体产生强烈的病毒特异性T细胞应答及体液免疫应答。更为重要的是该研究团队利用此小鼠模型评价了新冠感染康复者血浆和瑞德西韦对新冠病毒感染的治疗作用。结果显示,给予血浆治疗和药物组的小鼠肺脏病毒滴度均明显降低,且病理损伤减轻(见图3)。
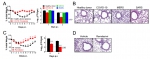
图3. 过继转移新冠康复者血浆和瑞德西韦治疗组,小鼠肺脏病毒滴度下降、肺脏病理损伤减轻。
模型优势:周期短、技术方法简单、适宜大规模推广,有利抗病毒药物、抗体、疫苗研究
赵金存介绍,该动物模型相比传统受体转基因小鼠模型,构建周期短(2-3周),不需要特殊繁育,可用于多种基因修饰小鼠动物模型构建;且技术方法简单,易于重复,适宜大规模推广,有利于我国抗病毒药物、抗体、疫苗的应急验证及致病机制研究,并已给我国多家单位广泛共享,有效缓解了我国新冠肺炎动物模型缺乏的难题。
据悉,赵金存教授为该研究第一通讯作者(Lead Contact),爱荷华大学Stanley Perlman和Paul B. McCray, Jr教授为研究共同通讯作者,广州医科大学附属第一医院/呼吸疾病国家重点实验室孙静博士、庄珍博士、刘冬兰博士、朱爱如博士、肇静娴博士、席寅博士,爱荷华大学郑健博士、李堃博士、Roy Lok-Yin Wong博士,广州海关技术中心黄吉城博士、李小波博士,以及广州再生医学与健康广东省实验室何江平博士为研究的并列第一作者。
该项目得到了国家重点研发计划(2018YFC1200100)、国家科技重大专项(2018ZX10301403)、科技部SARS-CoV-2防治应急专项(2020YFC0841400)以及广东省新发突发传染病防治专项(2020B111108001,2018B2020207013)等项目的资助。
(论文链接:https://www.cell.com/cell/fulltext/S0092-8674(20)30741-8?rss=yes)
广州日报全媒体记者 方晴 黎慧莹 王燕 骆昌威